研究内容:幹細胞再生修復医学分野(幹細胞生物学・再生医学)
幹細胞再生修復医学分野では、血液細胞のもとになる造血幹細胞の自己複製と分化のメカニズムを明らかにすることを目標としています。
また、同じ骨髄にいる、骨・脂肪・軟骨などのもとになり、造血幹細胞のサポートもする間葉系幹細胞による再生医療への応用研究も行っています。
骨髄ニッチは、ニッチ細胞(支持細胞)、およびニッチ細胞から産生される分子(ニッチ分子)から成ります。造血幹細胞のニッチとしては、骨内膜表面、細動脈、骨髄洞のニッチが同定されており、これらのニッチは間葉系幹細胞・血管・骨芽細胞・神経を含む多くの種類の細胞により構成されることが明らかになっています。
1. ニッチ分子の機能解析
幹細胞は幹細胞を2個生み出す対称分裂、幹細胞と分化した前駆細胞を1個ずつ生み出す非対称分裂、さらに2個の前駆細胞を生み出す対称分裂を行います。これらの細胞分裂パターンの制御は、組織中の幹細胞の数をコントロールする上で極めて重要です。我々は、造血幹細胞の対称分裂・非対称分裂の制御に関して、ニッチからのシグナルが重要な役割をもつと考えています。造血幹細胞の自己複製の分子機構を理解し、これを幹細胞増幅に繋げるためには、幹細胞の細胞分裂制御機構を明らかにする必要があり、造血幹細胞とニッチ細胞との相互作用が細胞分裂の制御にいかにして関わっているのかを明らかにすることは非常に興味深い課題となっています。
そこで我々は、1個の幹細胞から生じる2個の娘細胞 (paired daughter cell: PDC) について、1細胞レベルの網羅的遺伝子発現解析を行い、数学者と連携し、機械学習モデルを用いて遺伝子発現のパターンを解析することにより、対称・非対称分裂を識別・分類することが可能な解析系を確立しました。これを用い、Angpt1を介した造血幹細胞の細胞分裂制御機構の一端を解明しました(Arai F, 2020; Stumpf PS, 2021)。

図1.分裂様式から見たニッチ因子に対するHSCの機能変化
この研究では、造血幹/前駆細胞の遺伝子発現パターンを人工ニューラルネットワーク(ANN)に学習させ、細胞の種類を正確に識別し、細胞の年齢を予測する数学的モデルを作りました。その後、HSCの分裂直後の娘細胞を比較し、個々のHSCの自己複製能力が年齢とともに低下することが分かりました。さらに、HSCの細胞分裂は年齢によって性質が変化し、中年期では特にニッチ因子に対する感受性が変化する傾向が見られました。これらの結果から、幹細胞活性の内因性調節と外因性調節のバランスが年齢と共に変化し、幹細胞数は増える一方で再生能力が低下する理由と考えられます。
(Arai F et al., Cell Syst. 2020)
高度に純化し、一見均一に見える幹細胞であっても、実際にはヘテロな集団であることが明らかになってきました。そのため、幹細胞を集団として扱うのではなく、個々の細胞を対象として、ニッチの機能を解析することが重要となっています。特に、1細胞レベルの機能解析は、従来の手法では捉えることが難しい、個々の細胞の振る舞いを知ることができ、その結果、ニッチ全体の機能制御を明らかに出来ると考えております。この研究で培われた造血幹細胞ニッチの1細胞解析は他の幹細胞ニッチ研究のモデルにも成り得ると考えています。
2. 造血幹細胞の体外維持
造血幹細胞は組織幹細胞の中で最も解析の進んだものの1つであり、その維持に関わる分子群の同定および機能解析も進んでいます。しかしながら、試験管の中で機能的な造血幹細胞として維持しながら遺伝子操作することは未だ難しいとされています。これを達成するためには、ニッチシグナルの操作、ニッチを試験管内に再構築すること、遺伝子操作方法の最適化が重要な課題といえます。
このような課題を達成するためには、医学生物学のみならず、組織工学など他分野との緊密な連携が肝要であると考えます。我々は、生体工学領域の研究者との国際共同研究により、人工ニッチの作製に取り組んでいます。これまでに、ポリエチレングリコール・ハイドロゲルを用いて作製した人工ニッチ上で造血幹細胞の培養を行い、造血幹細胞数を増加させることが出来ることを細胞分裂解析によって確認しています。現在は、さまざまなニッチ分子で人工ニッチを修飾することで、生体の造血環境を再現し、造血幹細胞の増幅を達成したいと考え、研究を進めています。
我々は造血幹細胞において、ニッチ分子の1つであるAngpt1の刺激により、Shelterin複合体構成因子の1つ、Protection of telomere 1a (Pot1a) の発現が亢進することを見出しました。Pot1aは造血幹細胞のテロメア領域におけるDNAダメージの抑制、自己複製能の維持、老化制御に関わることを明らかにしています。さらに、細胞膜透過性Pot1a蛋白を用いて造血幹細胞にPot1a/POT1タンパクを造血幹細胞に導入する系を確立し、Pot1a/POTの導入により、機能的なマウスおよびヒト造血幹細胞を維持できることを見出しています(Hosokawa K, 2017)。

図2.HSCの維持に対する外因性Pot1aの機能
定常状態において、HSCはゆっくりと分裂と自己複製を繰り返しますが、老化が進むにつれて、HSCではテロメアDDRの蓄積とBMの再構成能力が低下します。同様の問題は、HSCの増殖中にも発生します。HSC内のPot1aレベルはこれらのプロセスによって低下しますが、外因性のPOT1a添加によって回復し、HSCの活性の喪失から保護されます。
(Hosokawa K et al., Nat Commun. 2017)
(Hosokawa K et al., Int J Hematol. 2018)
3. 造血幹細胞ニッチ・ニッチ分子の同定
我々は、造血幹細胞またはニッチ細胞特異的分子のレポーターマウスを用いた三次元骨髄イメージングを行い、造血幹細胞と周囲の細胞との立体的位置関係から、活性化した幹細胞と静止造血幹細胞について、それぞれ特異的なニッチを同定し、さらに、そのニッチ構成細胞を分離して、その特性を解析することで、造血幹細胞の活性化(増殖)⇔静止化を制御するメカニズムを明らかにしたいと考えています。
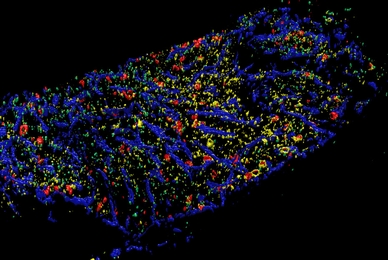 図3.マウス胸骨骨髄組織の3D蛍光イメージング
図3.マウス胸骨骨髄組織の3D蛍光イメージング
青:VE-carherin,
赤:CD150,
黄:Lineage/CD41/CD48,
緑:GFP
未分化造血幹細胞の生体組織内での局在をスピニングディスク共焦顕微鏡により鮮明に可視化することができ、幹細胞-ニッチ細胞の3次元解析を行います。
 図4.マウス頭蓋骨骨髄内の蛍光生体イメージング
図4.マウス頭蓋骨骨髄内の蛍光生体イメージング
青:VE-carherin,
白:GFP
生きた個体の中で、生きた細胞や分子の胴体を単一細胞単位で可視化することのできる「蛍光生体イメージング」は非常に強力な研究ツールです。3次元的解析に加え、時間軸を加えた4次元的な解析を行います。
血管内を移動していくGFP陽性の血球細胞を確認することができます。
(別ウインドウで動画がご覧になれます)
最近我々は、骨髄ニッチ細胞である間葉系幹細胞(MSC)のシェルタリン因子Pot1aの役割に関して研究を進めたところ、MSCの機能維持における重要性を明らかにしました(Nakashima K 2023)。このことから造血系だけでなく、他の組織幹細胞においても重要であることが考えられ、さらなる研究を進めています。
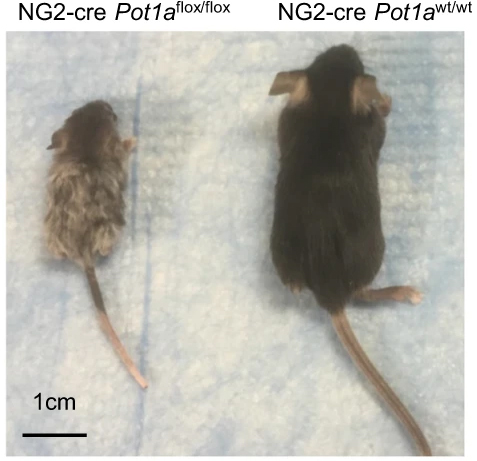
図5.NG2陽性細胞でPot1aを欠損したマウス
左)Pot1a欠損マウス、
右)同腹Controlマウス
NG2+MSCにおけるPot1aが、MSCの機能の維持に重要である他、B細胞分化制御、骨形成制御に関与することを明らかにした。
(Nakashima K et al., Commun Biol. 2023)

