研究内容:がん幹細胞医学分野(がん治療)
私たちは血液系のがん治療を目的として、その根源となっているがん幹細胞を標的とした研究を行っています。
現在、がん幹細胞において代謝や分子シグナルを制御することで、がんの増殖や発症に対する影響を明らかにしたいと考えています。
がん幹細胞ニッチの同定と制御
血液系腫瘍にも正常造血組織のように、基になるがん幹細胞が存在し、これらが薬剤・放射線療法に耐性を示すことが、がん再発に繋がると考えられています。
本研究では、がん幹細胞を支持するニッチ細胞を特定するため、遺伝子欠損マウスや造血器腫瘍モデルマウスを用い、ホールマウント3Dイメージングや、蛍光生体イメージングなどを行い、標的となる細胞の機能を解析しています。
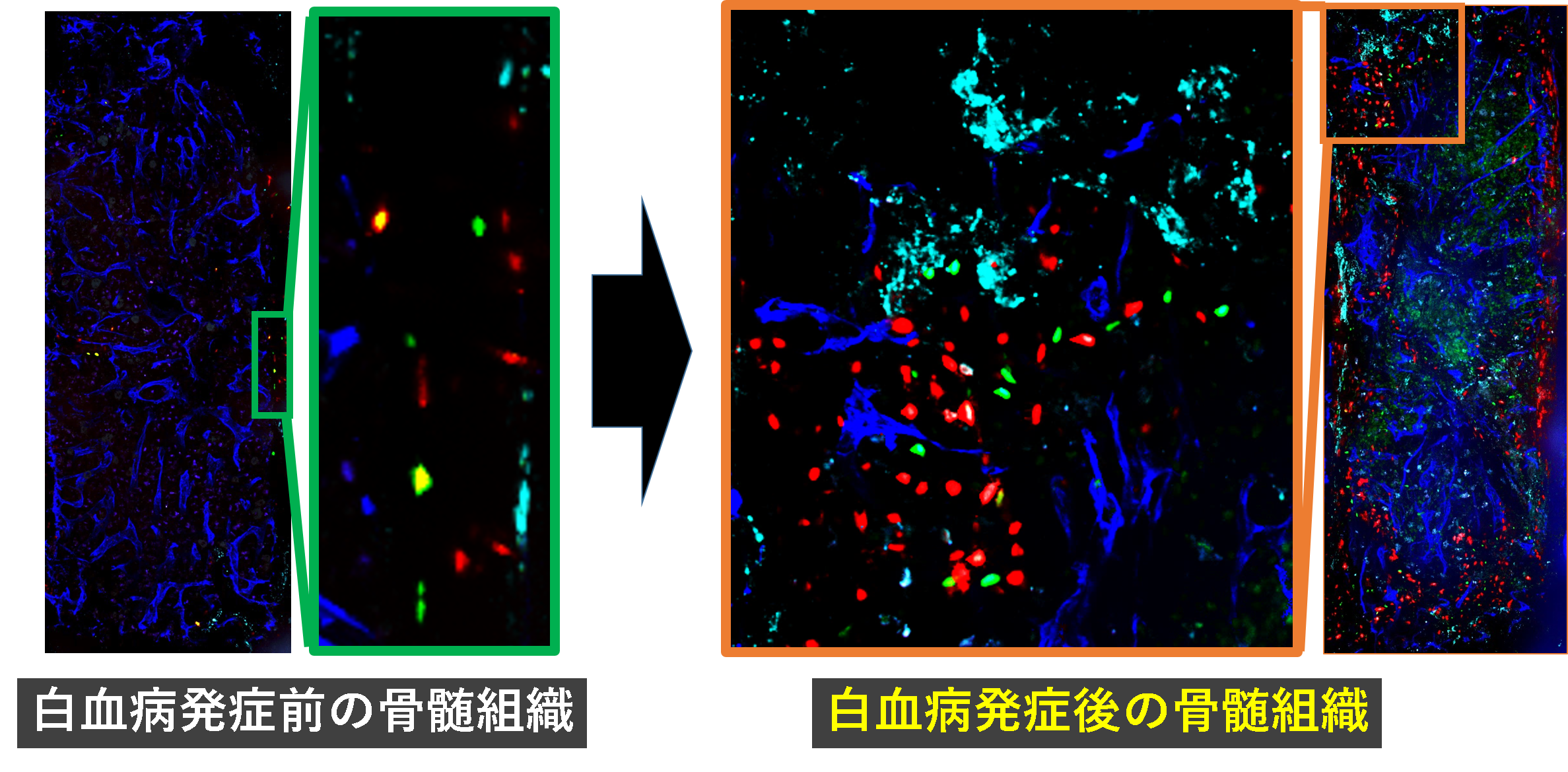
急性骨髄性白血病 (AML)の治療において、完全寛解後の再発は大きな課題となっています。この再発の主な原因の一つが白血病幹細胞 (LSC) の存在です。LSCは従来の化学療法に対して高い抵抗性を持ち、治療後も骨髄内に微小残存病変として生存することが明らかになっています。注目すべき点は、LSCがニッチと呼ばれる骨髄の微小環境に留まり、細胞周期を静止状態にすることで抗がん薬の作用を回避する特性を持つことです。この白血病幹細胞の特性により、患者が完全寛解に達した後でも、LSCが再び活性化して白血病細胞の増殖を引き起こし、再発に至ることがあります。したがって、AMLの根治的治療を実現するためには、LSCとその白血病ニッチを標的とした革新的な治療戦略の確立が必要です。
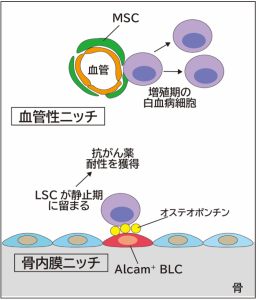
図1. 骨内膜ニッチは白血病幹細胞の静止状態を維持する
我々は、LSCが潜む白血病ニッチについて着目して白血病マウスモデルの解析を行い、骨内膜ニッチに存在する Alcam 陽性のbone lining cell (Alcam+ BLC) が、LSCを治療抵抗性の「静止状態」に維持する重要な役割を果たしていることを明らかにしました。細胞周期が静止期にあるLSCは、Alcam+ BLC が豊富な領域に集積していました。さらに、LSCから分泌される TGF-β1 が Alcam+ BLC のオステオポンチン (OPN) 産生を促進し、分泌されたオステオポンチンがLSCを骨内膜ニッチに留め、静止状態を維持するという TGF-β1/Tgfbr2/OPN シグナル経路を同定しました。これらの知見は、従来の化学療法では排除が困難であった静止期LSCを標的とした治療薬開発が可能になると期待されます。
(Ngan Thi Kim Nguyen et al., Leukemia, 2025)

